La TRANSPOSITION DES GROS VAISSEAUX (TGV)
Définition
La transposition des gros vaisseaux (TGV dans notre "jargon" médical) se définit par une inversion (transposition)
des gros vaisseaux sortant des ventricules, c'est-à-dire l'artère pulmonaire et l'aorte.
Dans un coeur normal, l'artère pulmonaire sort du ventricule droit et l'aorte sort du ventricule gauche (figure 1).
Le sang bleu, désoxygéné, en provenance du corps, arrive via les veines caves au coeur droit (oreillette et ventricule
droit) et est envoyé via l'artère pulmonaire vers les poumons où il est oxygéné. Il revient ensuite rouge car oxygéné, au
coeur gauche et est envoyé dans l'aorte afin d'oxygéner tous les organes et tissus. En cas de transposition des gros
vaisseaux, l'aorte sort du ventricule droit et l'artère pulmonaire du ventricule gauche (figure 2). Le sang bleu en
provenance du corps via les veines caves est donc renvoyé vers le corps via l'aorte tandis que le sang rouge en provenance
des poumons est renvoyé vers les poumons. Il y a donc deux circuits séparés, le rouge et le bleu, complètement inefficaces
ne permettant pas d'oxygéner les différents organes. Cette malformation est incompatible avec la vie en l'absence de
communications entre ces deux circuits (voir plus loin).
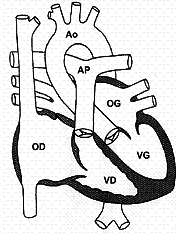 figure 1 : le coeur normal |
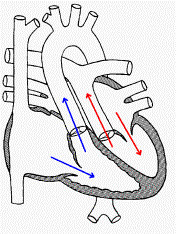 figure 2 : la TGV |
OD = oreillette droite, VD = ventricule droit, AP = artère pulmonaire, OG = oreillette gauche, VG = ventricule gauche, Ao = aorte
On parle de transposition "simple" lorsque celle-ci n'est pas associée à d'autres malformations majeures, comme une large
CIV (communication interventriculaire), une sténose ou atrésie pulmonaire, une coarctation ...
Ce chapitre traitera essentiellement de la transposition "simple" car les malformations associées peuvent fortement modifier
la présentation et la prise en charge.
Incidence
Rappelons que les malformations cardiaques sont présentes chez presque 1 % des nouveau-nés. La TGV représente la malformation
cardiaque cyanogène (c'est-à-dire provoquant une cyanose ou aspect bleu de l'enfant par manque d'oxygénation du sang artériel)
la plus fréquente à la naissance et représente 5 à 7 % des malformations cardiaques congénitales. Il y a une légère prédominance
masculine (60-70 % des cas sont des garçons).
Présentation clinique
Avant la naissance, le sang du foetus est oxygéné par le placenta et non par ses propres poumons. Par ailleurs, pendant
la vie foetale, deux communications intracardiaques sont normalement présentes : une communication interauriculaire (entre les
oreillettes) et le canal artériel (entre l'aorte et l'artère pulmonaire). Elles sont toutes deux nécessaires à la circulation
"normale" chez le foetus. La présence naturelle de ses communications avant la naissance permet au foetus porteur d'une TGV
d'être oxygéné correctement et donc de se développer harmonieusement. Il en résulte que l'enfant naît en général
avec une taille et un poids normaux, ce sont même souvent des gros bébés.
A la naissance, les poumons deviennent les "oxygénateurs" du sang. En présence d'une TGV, le sang oxygéné en provenance
des poumons sera renvoyé aux poumons au lieu d'être envoyé vers le corps. L'aorte ne recevra que du sang très bleu en
provenance des veines caves. L'enfant sera donc très cyanosé. Néanmoins, les premiers heures de vie, cette cyanose peut
être moindre par la persistance du canal artériel et de la communication entre les oreillettes (foramen ovale) permettant
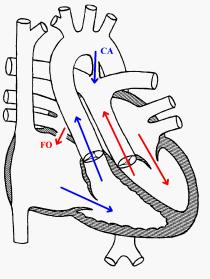
un certain mélange entre le sang bleu et rouge (figure 3). Cependant, rapidement (même parfois tout de suite après la
naissance), ces deux orifices auront tendance à se fermer. L'enfant deviendra alors extrêmement cyanosé. Cette cyanose
entraînera un manque d'oxygénation des différents organes d'où un mauvais fonctionnement de ces organes. En l'absence de
traitement approprié, ceci peut conduire au décès de l'enfant.
figure 3 : ce schéma montre les mélanges de sang entre la circulation "bleue" et "rouge" en cas de TGV, grâce au foramen ovale (FO) et au canal artériel (CA)
En cas de TGV simple, l'auscultation cardiaque ne mettra pas en évidence de souffle cardiaque. Autrement dit, si un nouveau-né est
très cyanosé, une auscultation cardiaque normale ne permet pas d'exclure une TGV.
Diagnostic
Une cyanose ne répondant que faiblement à l'oxygène administré, une absence de souffle cardiaque et certaines caractéristiques
à la radiographie du thorax permettront au pédiatre d'évoquer l'existence d'une TGV.
C'est l'échocardiographie qui permettra de poser le diagnostic de certitude.
Cet examen permettra aussi d'évaluer le degré d'ouverture du canal artériel et du foramen ovale et donc l'urgence d'un
traitement approprié. Il permettra également d'exclure d'autres anomalies associées. Un tiers des enfants avec TGV présentent
par ailleurs des anomalies des artères coronaires (figure 4), qui pourront parfois être dépistées par l'échocardiographie.
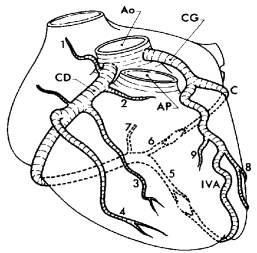
figure 4 : les artères coronaires naissent de l'aorte pour irriguer le muscle cardiaque.
Dans ce schéma, l'artère pulmonaire (AP) a été coupée pour dégager l'aorte (Ao), qui est aussi coupée au dessus de l'émergence des coronaires.
La coronaire gauche (CG) naît de la gauche de l'aorte et se divise en IVA (interventriculaire antérieure) et circonflexe (C), qui se dirige vers l'arrière.
La coronaire droite (CD) naît de la droite de l'aorte et se dirige vers le coeur droit.
En cas de transposition, il peut y avoir des anomalies coronaires associées, comme par exemple, la naissance de l'artère circonflexe de la
coronaire droite ou la présence d'une seule coronaire se divisant en trois etc ...
Diagnostic foetal (Dr C. Barrea) :
Actuellement il est possible de faire un diagnostic in utero (c'est-à-dire avant la naissance) de nombreuses malformations cardiaques au cours de
l'échographie morphologique de milieu de grossesse. La TGV est une malformation qui peut, en théorie, être dépistée in utero, mais ce n'est pas
toujours facile. Il n'est par ailleurs pas toujours possible de dépister les éventuelles anomalies associées et les coronaires ne sont, en
général, pas visibles in utero.
L'avantage de dépister cette malformation cardiaque in utero est de permettre l'organisation de la naissance de l'enfant dans un centre où il
peut être pris en charge immédiatement (parfois en salle d'accouchement même) et ce, sans devoir transférer l'enfant (et la maman) d'un
hôpital à l'autre. Ceci permet souvent d'éviter une cyanose trop importante et donc de réduire le risque de mauvaise perfusion des organes.
Il a été démontré scientifiquement que la mortalité autour de l'opération a nettement diminué grâce au diagnostic prénatal.
Prise en charge néonatale
Outre les soins "standards" de réanimation néonatale (oxygène, assistance respiratoire, perfusion de glucose (sucre) etc ...), nécessaires chez
certains enfants se présentant avec une TGV, deux traitements spécifiques seront indispensables :
1) la "prostaglandine E" (Prostin®) : ce médicament, disponible depuis les années 80, a révolutionné la prise en charge des
cardiopathies congénitales cyanogènes. Il permet de réouvrir le canal artériel qui, comme expliqué antérieurement, a tendance à se
fermer rapidement après la naissance. Ce médicament, qui doit être administré en perfusion intraveineuse continue, est présent dans toutes
unités de réanimation néonatale et peut donc être administré à l'enfant par le néonatologue avant le transfert de l'enfant dans un
hôpital spécialisé dans la prise en charge des enfants avec cardiopathie.
2) élargissement de la communication interauriculaire : si la communication interauriculaire est très petite, l'enfant restera cyanosé
même si le canal artériel est bien réouvert grâce au Prostin®. Il faudra alors procéder à un élargissement de cette
communication. Ceci ne se fait que dans les centres spécialisés dans la prise en charge des cardiopathies, par un cardiologue
pédiatre. Cette intervention s'appelle la septostomie selon Rashkind. Elle se fait en général aux soins intensifs, utilisant
l'échocardiographie pour guider la procédure. Le médecin insère une canule, soit dans la veine ombilicale (via l'ombilic-nombril)
soit dans la veine fémorale (pli de l'aine). A l'intérieur de cette canule est introduit un cathéter avec un ballonnet que l'on introduit
dans l'oreillette droite puis gauche via le petit trou restant. Le ballon est ensuite gonflé dans l'oreillette gauche, et un retrait assez
rapide du cathéter avec le ballon gonflé permet de déchirer la paroi entre les oreillettes et ainsi d'agrandir le trou (figure 5). Le cathéter
et le ballon sont retirés en fin de procédure.
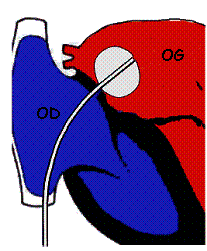
figure 5 : septostomie selon Rashkind :
le cathéter à ballon est avancé par le foramen ovale dans l'oreillette gauche (OG)
où le ballon est gonflé. Ensuite le cathéter est retiré vers l'oreillette droite (OD), ce qui déchire la paroi interauriculaire.
Ces 2 traitements, en améliorant l'oxygénation du bébé, permettent de stabiliser le bébé et d'attendre quelques jours jusqu'à l'intervention
correctrice.
Traitement chirurgical
Intervention selon Senning ou Mustard
C'était l'intervention systématiquement réalisée pour la TGV "simple" jusqu'à la fin des années 80. Après cela, son utilisation s'est limitée
aux enfants avec TGV et autres anomalies (y compris coronaires), rendant le switch artériel (cfr plus loin) impossible.
Cette intervention consiste à inverser le sang bleu et rouge au niveau des oreillettes. Le chirurgien va "tunneliser" les oreillettes de telle
façon à amener le sang bleu des veines caves vers le ventricule gauche qui se vide dans l'artère pulmonaire, et le sang rouge des veines
pulmonaires vers le ventricule droit qui se vide dans l'aorte (figure 6).
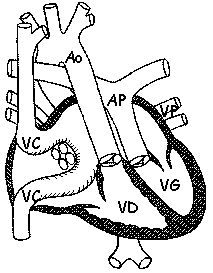
figure 6 : intervention selon Senning
Les veines caves (VC) sont dirigées vers le ventricule gauche (VG) qui éjecte dans l'artère pulmonaire (AP).
Les veines pulmonaires (VP) sont dirigées vers le ventricule droit (VD) qui éjecte dans l'aorte (Ao).
Même si cette intervention est actuellement souvent délaissée pour le "switch artériel", plus physiologique, elle a permis de sauver un grand
nombre d'enfants et leur a donné, et donne encore, une qualité de vie tout à fait satisfaisante. Il faut cependant se rendre compte que cette
intervention laisse un ventricule droit éjecter dans l'aorte. L'aorte est à pression plus élevée que l'artère pulmonaire et le ventricule droit n'est
normalement pas "programmé" pour travailler autant. Avec le temps, ce ventricule droit peut donc parfois montrer des signes de fatigue. Des contrôles
annuels sont donc recommandés après cette intervention afin de dépister et traiter de façon adéquate les éventuels signes de fatigue du ventricule
droit. Les cicatrices au niveau des oreillettes engendrées par le geste chirurgical peuvent également, avec le temps, favoriser des troubles du rythme,
pour lesquels des traitements peuvent être nécessaires.
Le switch artériel
Cette intervention consiste à inverser les grands vaisseaux. Autrement dit, l'aorte va être désinsérée du ventricule droit et
réinsérée sur le ventricule gauche et vice-versa pour l'artère pulmonaire (figure 7). Ceci est donc par définition plus physiologique
puisqu'elle remet les choses en place. Cette intervention est délicate car elle nécessite aussi la désinsertion et la réinsertion des
artères coronaires. C'est cette difficulté qui explique que cette intervention a mis tellement d'années avant d'être utilisée.
Cette intervention donne actuellement de très bons résultats, même si les risques ne sont jamais nuls (risques essentiellement liés à la
réinsertion des artères coronaires). Passé la période post-opératoire immédiate, ces enfants retrouvent une vie normale avec une tolérance
à l'effort normale. Les pratiques sportives à un très haut niveau de compétition restent néanmoins déconseillées pour ces enfants, comme après
toute intervention cardiaque.
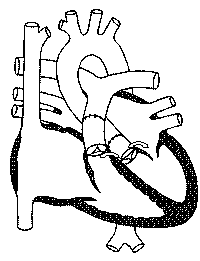
figure 7 : schéma montrant les sutures du switch artériel et les artères coronaires réinsérées.
Conclusion
La transposition des grands vaisseaux est une malformation cyanogène grave qui, en l'absence de traitement approprié, peut amener au
décès de l'enfant. Grâce aux progrès de la médecine (en particulier grâce à la disponibilité du Prostin® et la septostomie de Rashkind),
ces enfants sont à l'heure actuelle rapidement stabilisés. Les progrès des techniques chirurgicales permettent de rétablir une circulation
normale chez la grande majorité des enfants et d'offrir une qualité de vie normale.
(dossier réalisé par le Professeur Caroline Ovaert)